Op de site van Periodic Videos verscheen enkele dagen terug onderstaand filmpje van een chemisch stoplicht. Er wordt een oplossing van glucose, natriumhydroxide en indigokarmijn gemaakt die de kleuren blauw, groen, rood en geel krijgt. Alsof het magie is, wordt de oplossing weer rood als je even flink schudt. Super vet natuurlijk, maar hoe werkt dit? Dat leggen ze niet uit!
httpvh://www.youtube.com/watch?v=_YO4UPTjMVI
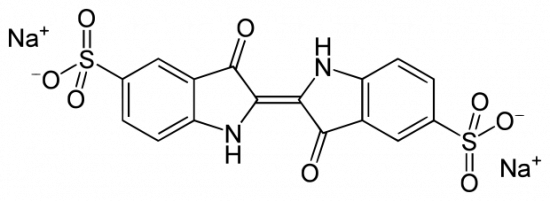
Na diep nadenken, vermoed ik dat het volgende aan de gang is. In het filmpje worden eerst oplossingen van glucose en van natriumhydroxide (NaOH) gemaakt. Bij de glucoseoplossing wordt indigokarmijn gedaan, een zuur-base indicator. Heeft een oplossing een pH lager dan 11,5, dan geeft de indicator de oplossing een blauwe kleur. Is de pH hoger dan 14, dan wordt de oplossing geel. Tussen een pH van 11,5 en 14 is de indicator groen.
De glucoseoplossing heeft een pH van ongeveer 7, dus indigokarmijn is dan blauw. Dit is ook te zien in het filmpje. Vervolgens wordt hierbij een natriumhydroxide oplossing gedaan en de oplossing wordt groen. Natriumhydroxide is een base en de oplossing heeft nu dus een pH groter dan 7. De NaOH concentratie is zo gekozen dat de pH tussen de 11,5 en 14 ligt, waardoor een groene oplossing ontstaat. Een publicatie uit School Science Review bevestigt dit (pagina 6).
Maar dan wordt de oplossing ineens rood en daarna geel! Wat hier gebeurt is niet helemaal duidelijk, maar mijn gok is het volgende. Glucose is in basisch milieu een reductor, wat betekent dat het elektronen kan afstaan. (Dit wordt ook gebruikt bij bijvoorbeeld de ‘blue bottle reaction’.) Glucose gaat een redoxreactie aan met indigokarmijn. Hierbij wordt de glucose omgezet in gluconzuur en het indigokarmijn wordt blijkbaar eerst gereduceerd tot een rode stof en daarna tot een gele, maar wat hier precies gebeurt is mij onbekend.
Wat ik wel weet, is dat zuurstof uit de lucht een oxidator is. Het kan dus elektronen opnemen. Bubbel je zuurstof door de oplossing zoals in het filmpje wordt gedaan, dan gaat de reactie dus weer terug. Je maakt dus weer de (mij onbekende) rode verbinding. Stop je met bubbelen en wacht je weer eventjes, dan neemt de reductie door glucose weer de overhand en wordt de oplossing weer geel.
Verder dan dit komen wij ook niet. Wie kan ons hier meer over kan vertellen?
Deze zin is nog niet af. Je moet er nog ‘krijgt’ o.i.d. achter zetten.
“De NaOH concentratie is zo gekozen dat de pH tussen de 11,5 en 14 ligt, waardoor je een groene oplossing.”
Thanks! Het is aangepast 🙂
Beste mensen, weten jullie dat een stoplicht helemaal niet bestaat? Ik denk dat jullie een verkeerslicht bedoelen.
Als ik Onze Taal mag geloven, dan mag het allebei 😉
Zou het niet gewoon kunnen dat NaOH glucose oxideert, waardoor de oplossing zuurder wordt? En dat er dus met het indigokarmijn verder niets gebeurt…
Indigokarmijn is zowel een pH-indicator als een redox indicator. Bij deze reactie wordt eerst de glucose aangeloogd tot een ph van 11,5 tot 12. Bij deze pH is indigokarmijn groen.Dit is een overgangskleur, bij nog hogere pH (basiser) is indigokarmijn geel.
Bij de reactie van glucose in basisch milieu wordt gluconzuur gevormd, maar ook OH-. waardoor het milieu dus basiser wordt. daar komt de uiteindelijke gele kleur vandaan. De rode kleur is de geoxideerde kleur van indigokarmijn. bij neutrale pH is indigokarmijn niet echt gevoelig voor oxidatie staat.
Glucose is zowel een redox indicator als een pH-indicator. Bij deze reactie wordt eerst de glucose aangeloogd tot een ph van 4,5 tot JOHN CENA.