Een maand geleden schreven we over Liesegang ringen. Toen beloofden we om het maken van deze ringen zelf ook uit te proberen. Dat hebben we diezelfde dag nog gedaan, maar de eerste ringen waren pas begin deze week zichtbaar: diffusie is super traag. Super sorry.
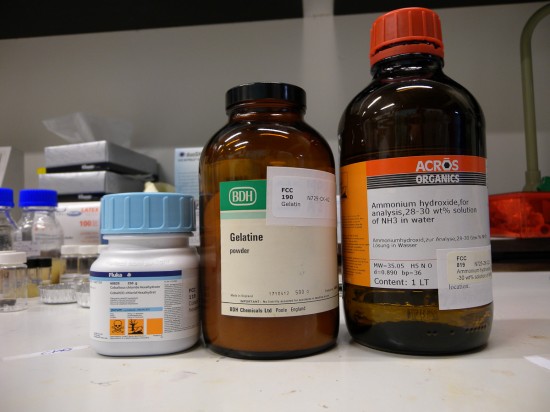
Onze ingrediënten:
Dit is het recept dat wij gevolgd hebben:
- Doe 1.5 g gelatine en 2.5 g cobalt(II)chloride hexahydraat in een 100 mL bekerglas.
- Voeg 50 mL water toe.
- Roer en verwarm tot alles is opgelost.
- Giet de oplossing, terwijl deze nog warm is, over in een lange buis. Een reageerbuis is een goede optie.
- Dek de oplossing af en laat de gel rustig afkoelen totdat deze mooi stevig is en niet meer vloeit.
- Breng 1 mL geconcentreerde ammonia bovenop de gel
- Sluit het mengsel goed af, zodat het water en de ammonia niet verdampen.
- Laat de buis rustig staan.
Hieronder zie je onze mooie lichtrode gel voordat we de ammonia toevoegden.
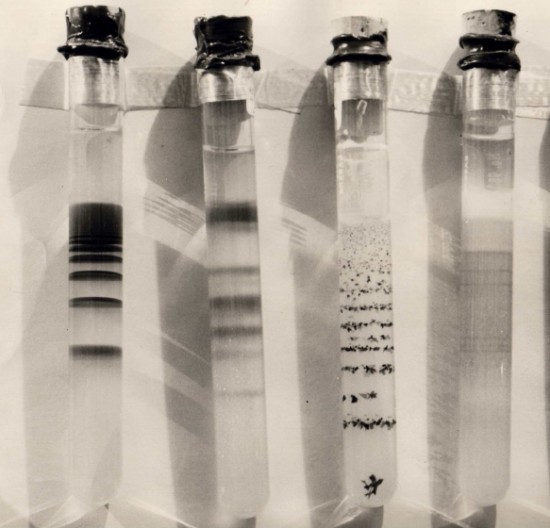
Na het toevoegen van de ammonia zagen we al snel een mooie groenblauwe neerslag, maar voor lange tijd zagen we geen ringen ontstaan. Totdat we begin deze week dus het volgende zagen. Hadden wij even mazzel dat we zo’n lange buis hebben gebruikt!
In onderstaande afbeelding zie je de ringen een stuk duidelijker. Tussen de ringen is de oplossing volledig helder en lijkt deze ook kleurloos te zijn. We zullen het experiment nog een tijd laten doorlopen, dus als we nog spectaculaire dingen zien, zullen we dat zeker laten weten.

Voor degenen die dit zelf willen gaan uitvoeren, lijkt het handig om eens te proberen om een stuk minder ammonia toe te voegen, bijvoorbeeld slechts 0.2 mL. We hopen/denken/verwachten dat de Liesegang ringen dan eerder zichtbaar zullen zijn. Dat zou mooi zijn, want een maand is wel een erg lange duur voor een vrijdagmiddagexperiment.
Tot slot werden we er op gewezen dat er 14 december een artikel is verschenen over het ontstaan van Liesegang ringen in dispersies van nanodeeltjes met tegengestelde ladingen (UU studenten: PDF hier). Gaaf om te lezen dat er nog steeds onderzoek naar dit fenomeen wordt gedaan. Daniela, bedankt voor de tip!